Modyfikacja właściwości powierzchni szklanych poprzez nakładanie powłok jest obecnie jedną z najprężniej rozwijających się dziedzin nowoczesnych technologii.
Ciekawym zagadnieniem naukowym jak również technologicznym, zainspirowanym odkrytym na początku lat dziewięćdziesiątych efektem kwiatu lotosu przez Wilhelma Barthlott’a i Christopha Neinhuis’a, jest wytworzenie na podłożu szklanym powłoki, charakteryzującej się wyjątkowymi właściwościami superhydrofobowymi.
Spełniającej wiele funkcji, do których należy zaliczyć np. efekt samoczyszczenia, czy efekt „niewidzialnej wycieraczki”.
Wprowadzenie
Artykuł stanowi próbę syntezy prac badawczych, pochodzących z ostatnich dwóch dziesięcioleci. Szczególną uwagę poświęca prezentacji modeli powłok hydrofobowych oraz podejmuje wyjaśnienia zjawisk zachodzących na granicy faz szkło-ciecz.
Ciała stałe, jak również różnego rodzaju materiały charakteryzują się zróżnicowanymi właściwościami powierzchniowymi. Jednym z istotnych parametrów opisujących powierzchnię ciała stałego jest hydrofobowość, gwarantująca odporność materiałów na wilgoć [1].
Materiały hydrofobowe nie są narażone na niszczące działanie wilgoci, a tym samym ich trwałość jest dużo większa. Brak właściwości hydrofobowych u szerokiej gamy produktów, niejednokrotnie ogranicza możliwości magazynowania, transportu czy stosowania ich w dziedzinach, w których mogłyby stanowić cenny surowiec ze względu na pozostałe swoje parametry.
W naturalny sposób ludzie od wieków chronią swoje otoczenie przed wilgocią. Początkowo używali do tego celu organicznych, hydrofobowych substancji, takich jak woski, tłuszcze itp., a na skutek intensywnego rozwoju nauki oraz technologii modyfikowali nowe materiały w kierunku nadania im właściwości wodoodpornych. Obecnie materiały o właściwościach hydrofobowych są stosowane zarówno w życiu codziennym, jak i w wielu dziedzinach przemysłu.
W przemyśle papierniczym do hydrofobizacji stosuje się tzw. środki zaklejające [2]. Podobnie w przemyśle górniczym do ochrony przeciwwybuchowej na szeroką skalę używany jest wodoodporny pył wapienny.
Konieczność ochrony obiektów budowlanych sprawiła, że właśnie w tym resorcie wykonano najwięcej prac badawczych o tematyce hydrofobizacji. Wnioski wyciągnięte na podstawie takich badań mogą być przenoszone na szereg innych dziedzin i materiałów.
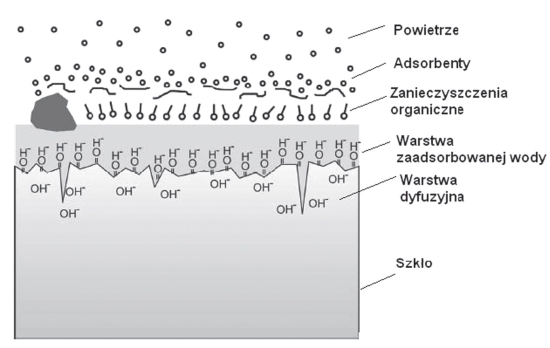
Rys. 1. Schemat budowy powierzchni szkła płaskiego
Pozwalają w prawidłowy sposób dobierać odpowiednie modyfikatory dla danego typu materiału, tak aby substancja hydrofobizująca łączyła się z modyfikowanym surowcem zmieniając jego właściwości elektrostatyczne oraz zakres występowania sił międzycząsteczkowych. Warunki prowadzenia procesu hydrofobizacji mogą również znacząco wpływać na jego przebieg.
Odpowiedni dobór takich parametrów, jak: temperatura, ciśnienie, stężenie środka hydrofobizującego i rozdrobnienie komponentów, ma duży wpływ zarówno na właściwości produktu, jak i sprawność oraz wydajność procesu. W literaturze można znaleźć szereg szczegółowych zaleceń prowadzenia procesu hydrofobizacji dla danego typu materiału.
Bardzo interesującym zagadnieniem badawczym jest opracowanie transparentnych powłok superhydrofobowych o podwyższonych właściwościach mechanicznych na powierzchni szkła sodowo-wapniowo- krzemianowego, powszechnie używanego jako szkło budowlane. Wspomniane powłoki hydrofobowe są szczególnie użyteczne w szybach budynków, pojazdów czy kolektorów słonecznych, ze względu na zwiększony efekt samoczyszczący oraz antyszronowy.
W dalszej części artykułu podjęto próbę omówienia różnych rodzajów warstw hydrofobowych, nanoszonych na powierzchnię szkła, a także wyjaśnienia charakteru oddziaływania międzycząsteczkowego na granicy faz warstwa-ciecz polarna (woda).
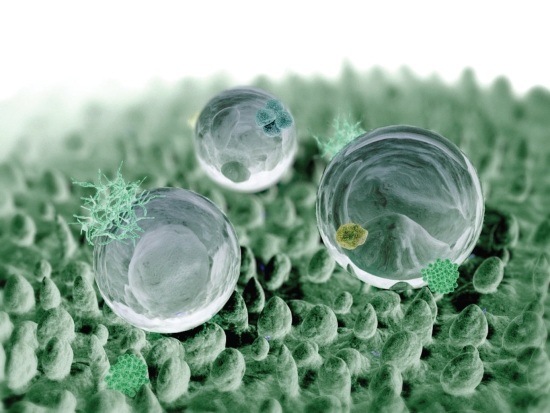
Rys. 2. Schemat mikrostruktury powierzchni liścia kwiatu lotosu
Omówienie zagadnienia
Pojęcie powierzchni szkła
W ujęciu fizycznym pod pojęciem powierzchni należy rozumieć rzeczywisty obraz budowy ciała stałego rozpatrywany w skali makro- i mikro-, który jest efektem nieciągłości, wynikającej z obecności szczelin, porowatości i innych defektów struktury.
Natomiast w aspekcie fizykochemicznym istotnym, dodatkowym parametrem jest zdefiniowanie wpływu oddziaływań ze strony środowiska zewnętrznego. Warto wspomnieć tu o heterogenicznej strefie rozciągającej się pomiędzy dwiema fazami ciągłymi (ciało stałe-gaz, ciało stałe- ciecz), które zachowuje swoją odrębność pod względem budowy i właściwości [3].
Atomy, cząsteczki oraz jony w warstwie wierzchniej ciała stałego – szkła – są rozmieszczone inaczej niż w jego wnętrzu, posiadają one większą energię potencjalną, zatem każdy kontakt powierzchni z inną fazą wyzwala procesy, prowadzące do zmniejszenia tej energii. Szybkość absorpcji gazów lub cieczy na powierzchni jest znacznie większa niż adsorpcja atomów, jonów i cząsteczek do wnętrza szkła [4, 5].
W wyniku różnej budowy warstwy wierzchniej, procesy zmieniające powierzchnię szklaną zachodzą samoistnie lub mogą być indukowane sztucznie.
Osadzanie na powierzchni warstw spowalnia procesy absorpcji, modyfikując w pożądany sposób ich parametry.
Schematyczny obraz opisywanego zjawiska zaprezentowano na rys. 1.
Skład chemiczny powierzchni szkła
Charakterystyczną cechą powierzchni szklanych jest obecność niewysyconych wiązań Si-O-, bądź też cząsteczek o budowie asymetrycznej, z częściowo przesuniętym ładunkiem elektrycznym o charakterze polarnym.
W zależności od składu chemicznego podłoża szklanego na powierzchni pojawiają się siły oddziaływań dążące do utworzenia wiązań chemicznych z molekułami lub jonami roztworów czy gazów. Najsilniejszymi z nich są oddziaływania jonowe, rzadziej natomiast pojawiają się oddziaływania elektrostatyczne lub będące efektem wewnątrzcząsteczkowego przenoszenia elektronu (oddziaływania typu donor-akceptor) [5, 6].

Rys. 3. Obraz SEM warstw o strukturze hierarchicznej, zbudowanej z mikrocząstek cynku oraz nanocząstek krzemionki, charakteryzującej się właściwościami superhydrofobowymi, z kątem zwilżania 1500 [30].
Zwilżalność powierzchni szkła, a hydrofobowość
Polarna powierzchnia w kontakcie z roztworem wodnym oddziaływuje z molekułami rozpuszczalnika, czyli wody, wyługowując alkalia. Drugim rodzajem oddziaływań pomiędzy hydrofilową powierzchnią szkła, a wodą są oddziaływania międzycząsteczkowe, do których należą siły międzyjonowe, siły van der Waalsa oraz oddziaływania EDA (elektronowo-donorowo-akceptorowe) i oddziaływania mostkowe (tlenowe i wodorowe). Dlatego też określenie charakteru powierzchni hydrofilowej jest wartością uśrednioną wielu parametrów [6, 7].
Zachowanie powierzchni hydrofobowej zdeterminowane jest przede wszystkim przez obecność w warstwie wierzchniej organicznych łańcuchów alifatycznych lub związków aromatycznych, zbudowanych z grup CH2 i CH3 lub też grup fluoroorganicznych CF2. W środowisku wodnym dipole rozpuszczalnika oddziaływują z łańcuchami organicznymi tylko na skutek pojawiających się sił van der Waalsa, natomiast brak jest interakcji donor-elektron, akceptor-elektron [8, 9].
Pokrycie szkła warstwą organiczną, charakteryzującą się wysokim stężeniem grup hydroksylowych, niepolarnych, zdolnych do szybkich ruchów rotacyjnych, czy w konsekwencji intensywnego tworzenia się sił dyspersyjnych, może powodować powstanie chwilowych dipoli i dipoli indukowanych (tzw. siły Londona) [9]. Zjawisko to może w bezpośredni sposób przyczynić się do zmiany charakteru powierzchni z hydrofobowej na hydrofilową [10].
Z pojęciem zwilżalności ściśle koresponduje termin energii powierzchniowej [11]. Obecnie uważa się, że wartość energii powierzchniowej jest parametrem bardziej precyzyjnym niż zwilżalność, ponieważ daje możliwość odpowiedzi na pytanie, o względnej wielkości składowych polarnej i niepolarnej [11-15].
Zgodnie z fizykochemiczną definicją swobodna energia powierzchniowa γ, jest równa pracy potrzebnej do utworzenia nowej jednostki powierzchni S i opisuje ją przedstawiona poniżej zależność:
γ=σ-S·(dγ/dS) (1)
Gdzie:
σ – napięcie powierzchniowe, siła styczna do danej powierzchni działająca na jednostkę długości
γ - swobodna energia powierzchniowa
Przy założeniu dγ/dS=0 i S≠0 wartość swobodnej energii powierzchniowej jest równa napięciu powierzchniowemu γ = σ, warunek ten jest spełniony, gdy adsorpcja na granicy faz lub potencjał chemiczny każdego ze składników układu jest równy zero [16].
Przegląd literatury
W przeciągu ostatnich dwudziestu lat, wielokrotnie podejmowano próbę wytworzenia superhydrofobowych warstw na szkle płaskim, bazujących na strukturze hierarchicznej podobnej do struktury liścia kwiatu lotosu [21] (na rys. 2 przedstawiono w sposób schematyczny przykład wspomnianej mikrostruktury), zbudowanej z części organicznej, polimerowej oraz nieorganicznej, zazwyczaj krzemionkowej [21, 22]. W tym celu wykorzystano szereg metod syntezy, takich jak metodę zol-żel, osadzania atomowego, napylania elektrostatycznego oraz różnego rodzaju techniki próżniowe, implantacji jonowej oraz nanolitografii [23-28].
Vinogradova w pracy Slippage of water over hydrophobic surfaces [29] podkreśla istotę doboru odpowiedniego składu chemicznego oraz otrzymanie pożądanego stopnia chropowatości powierzchni na właściwości hydrofobowe oraz parametry mechaniczne otrzymanych warstw. Wskazuję na zastosowanie do tego celu różnych pochodnych polidimetylosiloksanów, takich jak metylotrietoksysilan, czy decylotrimetyloksysilan oraz pochodne alkoksyflorosilanów.
Warstwa żelowa otrzymana z użyciem powyższych prekursorów, po wyżarzeniu charakteryzuje się strukturą nanokrystaliczną, o odpowiednim stopniu chropowatości powierzchni [30]. Na rys. 3 zaprezentowano mikrostrukturę cienkich powłok, o właściwościach superhydrofobowych z widoczną strukturą hierachiczną [30].
Suresh Kumar [31] wspomina o strukturach hierarchicznych warstw na szkle otrzymanych metodami elektrochemicznymi, z nanodendrytycznymi cząstkami złota lub srebra na powierzchni. Otrzymane powłoki charakteryzują się wysokim kątem zwilżania powyżej 1200 oraz zwiększoną odpornością na działanie środowisk agresywnych.
Zastosowanie powłok kompozytowych, składających się z części polimerowej oraz nieorganicznej np. z ZnO lub innych tlenków takich jak: TiO2, SnO2, WO3, V2O5, w odpowiednim środowisku chemicznym daje możliwość uzyskania powierzchni multifunkcyjnej, ze zmiennym charakterem zwilżalności zarówno hydrofobowym jak i hydrofilowym oraz odpornej na działanie substancji niepolarnych olejów, tłuszczów itp., zapewniającej efekt oleofobowy [32-35].
Powłoki hydrofobowe znajdują szerokie spektrum zastosowań, występują praktycznie w każdej dziedzinie życia. Poważnym problemem jednak dla takich warstw jest stosunkowo niska odporność na zarysowania i uszkodzenia mechaniczne. Dlatego wyzwaniem dla inżynierii materiałowej jest opracowanie skutecznej techniki nakładania powłok hydrofobowych. Istotnym problemem jest także stabilizacja nanostruktur w cienkiej warstwie oraz wyznaczenie optymalnego składu chemicznego stosowanych prekursorów wyjściowych.
Wnioski
Powłoki hydrofobowe na szkle, powszechnie nazywane „niewidzialną wycieraczką” znajdują zastosowanie praktycznie w każdej dziedzinie współczesnego życia. Od pół wieku, prowadzone są liczne prace badawcze mające na celu wyjaśnienie zjawisk zachodzących na granicy faz warstwa-ciecz polarna, poprawę parametrów i obniżenie kosztów produkcji powłok.
Bardzo skomplikowanym problemem naukowym jest otrzymanie warstwy hydrofobowej o dobrych parametrach wytrzymałościowych, odpornej na działanie silnych środków chemicznych. Takie powłoki nanoszone na szklane podłoża, charakteryzujące się dobrymi właściwościami mechanicznymi, powinny posiadać w swojej budowie zarówno grupy organiczne-polimerowe, jak i nieorganiczne nanostruktury, np. krzemionkowe. Syntezy warstw w takich układach przyczyniają się do powstania struktur hierarchicznych, zwiększających parametr chropowatości.
Warstwy hydrofobowe powinny charakteryzować się niską swobodną energią powierzchniową oraz spadkiem polarnego charakteru powierzchni, wówczas odpychają one bardzo skutecznie cząsteczki wody i innych roztworów.
Pionierskim rozwiązaniem zaistniałego problemu, wydaje się zastosowanie metod elektrostatycznego osadzania warstw na powierzchni szkła, które gwarantuje odpowiedni wzrost hierarchicznych nanostruktur, o odpowiednim stopniu chropowatości, o bardzo dobrych parametrach mechanicznych, oraz wysokiej odporności na ścieranie.
mgr Joanna Zontek
Katedra Technologii Materiałów
Budowlanych, AGH, Kraków
e-mail:
prof. dr hab. inż. Jan Wasylak
Katedra Technologii Materiałów
Budowlanych, AGH, Kraków
Literatura
[1] A. Hozumi, K. Ushiyama, H. Sugimura, O. Takai, 1999 Langmuir 15 s. 7600.
[2] F. Cossement, F. Plumier, J. Delhalle, L. Hevasi, Z. Mekhalif, (2003) Synth. Met. pp.138 529.
[3] Saint-Gobain, Patents No. US 6,340,502 B1 (2002) and No. US 6,451,432 B1
[4] J. Simonet, in: H. Lund, M.M. Baizer (Eds.), 1990, Organic Electrochemistry, 3rd ed., Marcel Dekker, New York, s. 1253.
[5] K. Brace, C. Combellas, E. Dujardin, A. Thiebault, M. Delamar, F. Kanoufi, 1997, ´M.E.R. Shanahan, Polymer 38 s. 3295.
[6] L. Kavan, in: P.A. Thrower (Ed.), 1991, Chemistry and Physics of Carbon, Marcel Dekker, New Yorkp. 71.
[7] C. Combellas, F. Kanoufi, H. Marzouk, A. Thiebault,1995, French Patent No. ´95 09726.
[8] C. Combellas, J. Ghilane, F. Kanoufi, D. Mazouzi, 2004, J. Phys. Chem. B 108 s.6391.
[9] C. Combellas, F. Kanoufi, D. Mazouzi, 2004, J. Phys. Chem. B 108 s.19260.
[10] C. Combellas, M. Fermigier, A. Fuchs, F. Kanoufi,2005, Anal. Chem. 77, s. 7966.
[11] C. Combellas, F. Kanoufi, D. Mazouzi, J. Electroanal., 2006,Chem. 589 s. 243.
[12] C. Combellas, A. Fuchs, F. Kanoufi, 2006, French Patent .No. 05 05704,
[13] M.E.R. Shanahan,1999, Colloids Surf. A 156 s.71.
[14] C. Combellas, A. Fuchs, F. Kanoufi, M.E.R. Shanahan, in: K.L. Mittal (Ed.), 2006, Contact Angle, Wettability and Adhesion, vol. 4, V.S.P, Utrecht, s.43.
[15] F. Kanoufi, C. Combellas, M.E.R. Shanahan, 2003, Langmuir 19 s. 6711.
[16] S. Wu, 1982, Polymer Interfaces and Adhesion, Marcel Dekker, New York,.
[17] D.Y. Kwok, A.W. Neumann, 1999, Adv. Colloid Interf. Sci. 81 s.167.
[18] F.M. Fowkes, 1964, Ind. Eng. Chem. 56 s. 40.
[19] R.N. Wenzel, 1936, Ind. Eng. Chem. 28 s. 988.
[20] A.B.D. Cassie, S. Baxter, 1944, Trans. Faraday Soc. 40 s.546.
[21] M.E.R. Shanahan, in: K.W. Allen (Ed.) ,1991, Adhesion 15, Elsevier Applied Science, Londonp. 116.
[22] T. Pompe, S. Herminghaus 2000, Phys. Rev. Lett. 85, s. 1930.
[23] J.F. Joanny, P.G. de Gennes ,1984, J. Chem. Phys. 81, s. 552.
[24] M.E.R. Shanahan, 1990, J. Phys. D: Appl. Phys. 23 s.703.
[25] J.A. Marsh, A.M. Cazabat, 1993, Europhys. Lett. 23 s. 45.
[26] K. Luo, M.P. Kuitti, C. Tong, S. Majaniemi, T. Ala-Nissila 2005, J. Chem. Phys.123 s.194702.
[27] M.O. Robbins, J.F. Joanny,1987, Europhys. Lett. 3 s. 729.
[28] S.B. Haderleln, R.P. Schwarzenbach, 1993, Adsorption of substituted nitrobenzenes and nitrophenols to mineral surface, Environ. Sci. Technol. 27, s. 316–326.
[29] K. Sugiyama, K. Fukunaga, Y. Kuramochi, A. Iwata, S. Nishijima, S. Takeda, A.Nakahira, 2000, Oil spill recovery method using magnetic material by magnetic separation, JP -176306
[30] K. Sever, M. Sarikanat, Y. Seki, V. Cecen, I.H. Tavman, 2008, Effect of fiber surface treatments onmechanicalproperties of epoxy composites reinforcedwithglass fabric, J. Mater. Sci. 43 s. 4666–4672.
[31] A.G. Casado, E.J.A. Hernández, P. Espinosa, J.L. Vílchez, 1998, Determination of total fatty acids (C8–C22) in sludges by gas chromatography-mass spectrometry, J. Chromatogr. A 826, s.49–56.
[32] E.F. Joy, A.J. Barnard Jr., Standard Methods of Chemical Analysis, in: F.J.Welcher (Ed) 1963, Commercials Acids and Bases, vol. 2, 6th ed., D. Van Nostrand, New Jersey, s. 580–581.
[33] A.F.M. Barton, 1983, CRC Handbook of Solubility Parameters and Other Cohesion Parameters, CRC Press, Inc., Boca Raton, FL.
[34] F.D. Lewis, B. Holman,1980, Singlet states of benzonitrile and pdimethylaminobenzonitrile, J. Phys. Chem. 84 2326–2328.
[35] I. Zilberberg, M. Ilchenko, O. Isayev, L. Gorb, J. Leszczynski, 2004, Modeling the gasphase reductionofnitrobenzene tonitrosobenzene by ironmonoxide: a densityfunctional theory study, J. Phys. Chem. A 108 pp.4878–4886.
Całość artykułu w wydaniu drukowanym i elektronicznym
inne artykuły o podobnej tematyce patrz Serwisy Tematyczne
więcej informacj: Świat Szkła 9/2012































